Marian Wiegand und Ulrike Protzer, München
Hepatitis B: Therapeutische Impfung in klinischer Entwicklung
Um
die Krankheitslast durch das Hepatitis-B-Virus (HBV) zu reduzieren,
hat die WHO einen Aufruf zum Handeln veröffentlicht. Das nachhaltige
Entwicklungsziel 3.3 der Vereinten Nationen zur Bekämpfung der
Virushepatitis zielt darauf ab, HBV als Gefahr für die öffentliche
Gesundheit zu bekämpfen und soll bis 2030 erreicht werden.
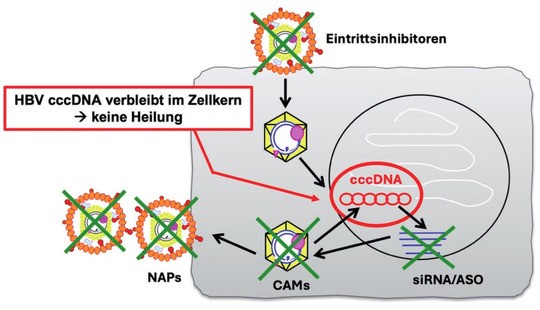
Abb. 1 Infizierte Leberzelle mit Viruspartikeln im Zytoplasma und der viralen cccDNA, die extrachromosomal im Zellkern vorliegt. Das Virus bietet in seinem Replikationszyklus, beginnend beim Eintritt in die Zelle, über die Replikation und Genexpression bis zum Zusammenbau und der Ausschleusung neuer Viruspartikel, verschiedene therapeutische Ansatzpunkte
Das zentrale Problem bei der Behandlung der chronischen HBV-Infektion (CHB) ist die Resistenz des HBV gegen eine Elimination, bedingt durch die Ablagerung einer stabilen Persistenzform des Virus im Kern infizierten Hepatozyten, der cccDNA (Abb. 1) sowie die Entwicklung einer HBV-spezifischen Immuntoleranz, die die Abtötung infizierter Leberzellen durch T-Zellen verhindert.
In seltenen Fällen kann eine chronische HBV-Infektion ausheilen, denn bei 0,5% der CHB-Patienten pro Jahr regeneriert sich die HBV-spezifische Immunität spontan: Antikörper gegen das HBsAg sowie polyklonale CD4- und CD8-T-Zell-Reaktionen werden nachweisbar. So kann z.B. eine Knochenmarktransplantation von HBV-immunen Spendern HBV bei chronischen Trägern heilen, was auf die Bedeutung der zellulären Immunität hinweist.
Funktionelle Heilung
Die derzeit verfügbaren antiviralen Behandlungen mit Nukleosidanaloga sind gut verträglich und kontrollieren die HBV-Replikation, heilen die HBV-Infektion jedoch nicht aus, da sie nicht die erforderliche Immunantwort zur Kontrolle der Infektion hervorrufen. Was fehlt, ist eine zeitlich überschaubare, kurative Behandlung, die spezifisch die Immunantwort des Wirts stimuliert, um HBV bei chronisch infizierten Personen zu kontrollieren und zu heilen, so dass die Notwendigkeit der langfristigen Gabe antiviraler Medikamente entfällt.
Die Ausheilung einer HBV-Infektion im Sinne einer „HBV cure“ oder „functional cure“, ist durch den HBsAg-Verlust im Serum und idealerweise durch eine anti-HBs-Serokonversion definiert, begleitet von einer anhaltenden (Immun-)Kontrolle der Virusvermehrung, trotz des Fortbestehens geringer Mengen an cccDNA in der Leber.
Chronische Hepatitis B weltweit
Trotz der Verfügbarkeit eines prophylaktischen Impfstoffs seit über 40 Jahren stellt die Infektion mit dem Hepatitis-B-Virus (HBV) nach wie vor eine große Gesundheitsgefahr dar. Weiterhin infizieren sich jedes Jahr ca. 1,2 Millionen Menschen mit dem HBV. Das HBV verursacht laut WHO jährlich 1,1 Millionen Todesfälle, zumeist infolge chronischer HBV-Infektion. HBV-Träger haben ein hohes Risiko, eine Leberzirrhose und ein hepatozelluläres Karzinom zu entwickeln. Weltweit sind mehr als 250 Millionen Menschen von einer chronischen HBV-Infektion betroffen, die sie häufig bereits seit der Kindheit in sich tragen. Ein Großteil der Betroffenen lebt in Südostasien (>70 Mio.), in China (>85 Mio.) und in Afrika (ca. 65 Mio.). Aber auch in Europa (>10 Mio.), im Mittleren Osten (>15 Mio.) und auf dem amerikanischen Kontinent (>5 Mio.) leben viele chronisch HBV-Infizierte. Bei etwa 8 Millionen Patienten wird eine chronische Hepatitis B durch eine Superinfektion mit dem Hepatitis-D-Virus (HDV) kompliziert, was das Risiko für Folgeschäden deutlich erhöht.
Die Blaupause für die funktionelle Heilung ist die „natürliche Ausheilung der HBV-Infektion“ durch die antivirale Immunantwort, die bei der Mehrheit der Erwachsenen mit akuter HBV-Infektion eintritt. Das Virus wird höchstens bei einer tiefgreifenden Immunsuppression reaktiviert. Ein vollständiger Verlust von HBsAg bei CHB-Patienten wird jedoch durch die Expression von HBs aus integrierten, wenn auch nicht funktionsfähigen, HBV-DNA-Kopien erschwert.
Aktuelle Konzepte
Gegenwärtig werden zwei Konzepte in der Therapieentwicklung gegen chronische Hepatitis B verfolgt:
Neben den verfügbaren Nukleosid-Analoga werden neue, direkt antiviral wirksame Medikamente (DAA – direct-acting antivirals) entwickelt, die bestimmte Schritte im viralen Lebenszyklus blockieren. Diese umfassen Inhibitoren des Viruseintritts, Kapsid-Assembly-Modulatoren, Nukleinsäure-Polymere, small-interfering (si)RNAs oder Antisense-Oligonukleotide (Abb. 1). Keines dieser DAAs greift jedoch die virale Persistenzform cccDNA an, die als Template für die Produktion neuer Virionen im Zellkern infizierter Hepatozyten deponiert wird und auch nach Jahrzehnten der Persistenz zu einer Reaktivierung führen kann. Daher können DAAs konzeptionell bedingt zwar die Infektion bzw. Viruslast kontrollieren, aber die HBV-Infektion nicht ausheilen und müssen dementsprechend langfristig verabreicht werden.
Im
Gegensatz zu DAAs stehen immuntherapeutische Ansätze, bei denen die
patienteneigene Immunantwort, die die Infektion kontrollieren soll,
stimuliert wird. Dabei gilt das Konzept einer „therapeutischen
Vakzine“, die eigentlich eine Immuntherapie ist, aktuell als einer
der vielversprechendsten Ansätze, um eine nachhaltige therapeutische
Wirkung zu erzielen.
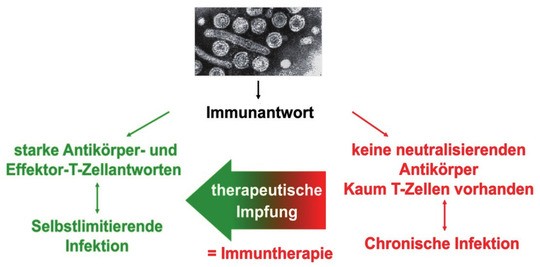
Abb. 2 Wirkungsweise einer therapeutischen Vakzine für die chronische Hepatitis B
Das Ziel einer therapeutischen Vakzine ist (Abb. 2):
(1) die Aktivierung einer ausbalancierten Helfer-T-Zell-Antwort, um sowohl B-Zellen als auch zytotoxische T-Zellen zu stimulieren und zu unterstützen.
(2) die Stimulation und Ausreifung von B-Zellen zur Produktion von neutralisierenden Anti-HBs-Antikörpern, um eine Infektion bisher noch nicht befallener Leberzellen zu verhindern.
(3) die Stimulation und Expansion von CD8+ „Killer“-T-Zellen, die HBV-infizierte Leberzellen sowie Zellen mit integrierter HBV-DNA eliminieren können, die als Tumor-Vorläufer gelten.
Dabei ist die zelluläre Immunantwort entscheidend für die langfristige Kontrolle und die Ausheilung der HBV-Infektion. Die T-Zellen eliminieren nicht nur HBV-infizierte Zellen, sondern regulieren durch Zytokine, die sie freisetzen, auch die HBV-Persistenz, Genexpression und Replikation des Virus. In experimentellen Arbeiten konnten wir zeigen, dass Zytokine, wie z.B. die Interferone, die von aktivierten Immunzellen freigesetzt werden, die cccDNA unterdrücken oder sogar degradieren können.
In Entwicklung
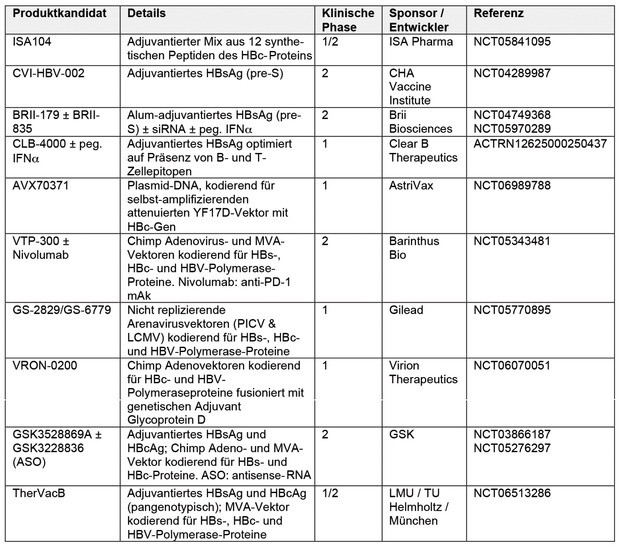
Tab. 1 Klinischer Entwicklungsstand von Immuntherapien bzw. therapeutischen Hepatitis B Vakzinen
Gegenwärtig befinden sich verschiedene spezifische Immuntherapien und therapeutische Vakzine in der Entwicklung (Tab. 1). Einige Ansätze verwenden nur HBsAg oder HBcAg als virusspezifisches Antigen (z.B. BRII-179, CVI-HBV-002, CLB-4000, ISA104, AVX70371), andere sind rein vektorbasiert (z.B. VTP-300, GS-2829/GS-6779, VRON-0200). Diese Ansätze bergen das Risiko, eine Immunantwort zu induzieren, die erstens nicht breit genug ist, da zu wenige immunogene Epitope der verschiedenen HBV-Antigene repräsentiert sind oder zweitens die spezifische Immunantwort entweder nur auf Antikörper- oder nur auf T-Zellen fokussiert ist. Das Zusammenspiel beider Arme der Immunantwort ist jedoch wichtig, um einerseits eine weitere Virusausbreitung zu unterbinden und andererseits infizierte Hepatozyten durch zytotoxische T-Zellen zu eliminieren.
Ansatz mit Vektor
Der vektorbasierte Ansatz VTP-300 wird in Kombination mit dem Checkpoint-Inhibitor Nivolumab (Anti-PD-1) getestet, wodurch die Wiederherstellung von T-Zell-Antworten in der Leber unterstützt werden soll. Daten aus einer abgeschlossenen Phase-1/2-Studie zeigten eine Verstärkung der Induktion einer HBV-spezifischen Immunantwort durch VTP-300 in Kombination mit Nivolumab bei Patienten mit niedrigem HBsAg, bei gleichzeitig guter Verträglichkeit. In der laufenden Phase-2b-Studie werden verschiedene Kombinationen bei einer größeren Zahl von Patienten getestet.
Ein
Ansatz der Firma GSK kombiniert Proteinantigene mit der Gabe viraler
Vektoren im heterologen Prime-
Boost-Ansatz (GSK3528869A). Die
Interimsanalyse der klinischen Phase-2-Studie zeigte keine
ausreichende Wirksamkeit, um die Studie fortzuführen. Anstatt dessen
wurde eine Kombination aus dem Prime-Boost-Ansatz und der Gabe des
Antisense-Oligonukleotids Bepirovirsen eingesetzt, das gezielt die
viralen RNA-Transkripte reduzieren soll.
Eine am Helmholtz Zentrum München entwickelte therapeutische Vakzine („TherVacB“) ist ebenfalls als heterologer Prime-Boost konzipiert, wobei sich das Antigendesign und die Adjuvantierung sowie das Vektordesign vom GSK-Ansatz unterscheiden. Zunächst wird zweimal eine Kombination aus HBsAg- und HBcAg-Partikel in Verbindung mit einem nukleosidischen Adjuvanz appliziert. Danach folgt eine Booster-Immunisierung mit einem MVA-basierten Vektor, der mehrere HBV-Antigene exprimiert. TherVacB wurde als pangenotypische Therapie entwickelt, indem die Impfstoffkomponenten HBcAg und der virale MVA-Vektor die Antigensequenzen verschiedener HBV-Genotypen abdecken. Damit kann TherVacB weltweit eingesetzt werden obwohl sich die HBV-Genotypen in den verschiedenen Regionen der Welt unterscheiden (Genotyp A: Nordamerika, Subsahara, Westafrika; C: Asien, Südost-Asien; D: Europa und Mittelmeerraum, Afrika, Indien).
Kombination besser?
Bisher veröffentlichte Ergebnisse aus ersten klinischen Studien konnten zeigen, dass Immuntherapien zu einer ‚Functional Cure‘ der chronischen Hepatitis B führen können. Generell sind nachhaltige Erfolgsraten noch gering, aber zumindest bei Kombinationstherapie vielversprechend. Insgesamt zeigt sich, dass niedrigere Ausgangs-HBsAg-Werte der Patienten (HBsAg ≤1.000IU/ml) einen Therapieerfolg wahrscheinlicher machen. Als Konsequenz werden u.a. Kombinationen von Immuntherapien mit antiviralen Therapien evaluiert, die gezielt das HBsAg-Level senken. Erste klinische Testungen laufen gegenwärtig für zwei Programme (s. Tab. 1: BRII-179 + BRII-835 und GSK3528869A + GSK3228836), in denen siRNA bzw. ein ASO gegen die viralen RNAs eingesetzt werden. Weitere Kombinationen in anderen Programmen sind in Planung.
Fazit
Zusammenfassend lässt sich sagen, dass die Komplexität der Hepatitis-B-Infektion und die Persistenz des Virus im Zellkern die Entwicklung einer Therapie, die eine Ausheilung erlaubt, deutlich erschweren. Andererseits haben die weltweiten intensiven Forschungs- und Entwicklungsaktivitäten dazu beigetragen, gezielte Therapien zu entwickeln. Nach heutigem Kenntnisstand sind immuntherapeutische Ansätze wie z.B. eine therapeutische Vakzine wohl die vielversprechendsten. Sie dürften sich als essenzieller Bestandteil von Kombinationstherapien durchsetzen, die eine Heilung der chronischen HBV-Infektion ermöglichen.
Literatur beim Verfasser







 Diese Seite weiter empfehlen
Diese Seite weiter empfehlen