Martin Obermeier, Berlin und Dirk Berzow, Hamburg
HIV-2 – PLWH2 in Deutschland
Die Infektion mit HIV-2 unterscheidet sich in einigen Aspekten von HIV-1 Infektionen. Bei PLWH2 (Menschen, die mit einer HIV-2 Infektion leben), wird oft eine verlangsamte Krankheitsprogression beobachtet. Virämie und Höhe der Immunaktivitätsmarker sind bei HIV-2 geringer. In Studien gibt es einen signifikant größeren Anteil von LTNP (Long-Term-Non-Progressors) und EC (Elite Controllers) als bei HIV-1, wahrscheinlich abhängig von der Länge der Beobachtungszeit. Im afrikanischen Setting ist die Zeit bis zum Auftreten von AIDS etwa doppelt so lang (20 Jahre versus 10 Jahre bei HIV-1). Bei vielen Verläufen sind die Endpunkte dann aber doch gleich (Auftreten von HIV-assoziierten Krankheiten).
Bei HIV-2 gibt es auch bei der Therapie Besonderheiten. Die strukturellen Unterschiede zu HIV-1 sind auf Protein-Ebene 35 bis 55 Prozent, je nach Region (Faria et al. 2013). In der Folge ist ein Teil der antiretroviralen Substanzen nicht oder nicht ausreichend wirksam. Auch die Resistenzentwicklungswege unterscheiden sich zum Teil, was in der Therapieplanung zu beachten ist.
Es gibt in Deutschland ca. 100 bis 200 PLWH2.
Studie H2O
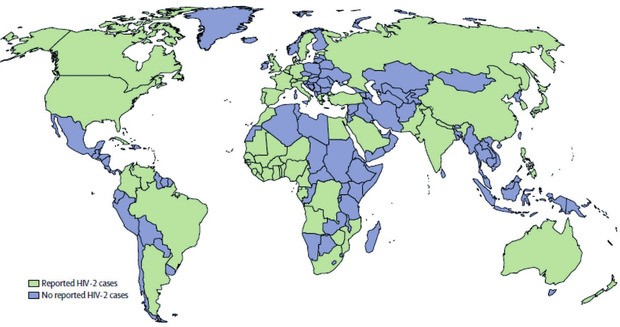
Abb. 1 Map of countries with reported HIV-2 cases – Countries or regions with reported HIV-2 cases are shown in green, Data are compiled from entries in the Los Alamos National Laboratory HIV database and country-specific searches for HIV-2 on PubMed (accessed March 16, 2018)
Seit 2020 werden Daten von PLWH2 retro- und prospektiv erhoben. Beteiligt sind zurzeit nur Hamburger Zentren, aber es ist eine Plattform in Arbeit, die die Teilnahme von weiteren Zentren ermöglichen wird.
Aktuell konnten Daten von 25 PLWH2 ausgewertet werden (12w/13m). Der Beobachtungszeitraum ist von 1998 bis 2025. Die „Observation time“ (OT) beträgt 338 Patientenjahre (mittlere OT 14 Jahre, Wertebereich 1-27 Jahre). Das Durchschnittsalter liegt bei 61 Jahren (46-83 Jahre). Die teilnehmenden PLWH2 stammen aus acht Ländern: Guinea-Bissau (10), Ghana (5), Deutschland (4), Gambia (2), Elfenbeinküste, Portugal, Togo, Türkei. Unter den Teilnehmenden gibt es eine HIV-1/HIV-2 Koinfektion. Es gab keinen Todesfall während der Beobachtungszeit. Drei Teilnehmende sind Lost-To-Follow-Up (LTFU) nach drei, fünf und sieben Jahren aus unbekannten Gründen.1
„Re-Controlling“?
Von den 25 teilnehmenden PLWH2 sind bis jetzt nur vier (16%) ohne ART verblieben (OT 1, 12, 15 und 21 Jahre). Diese Teilnehmenden zeigen keine Krankheitsprogression und sind immunologisch stabil. Virologisch verhalten sie sich aber nicht wie Elite Controller (EC): Die Daten zeigen mindestens einen „Blip“ bei allen vier „Controllers“ und Low-Level-Virämien bei drei der vier Teilnehmenden in dieser Gruppe (bis zu 100-200 cop/ml, z.T. >10 Monate). Danach sind sie wieder für längere Phasen avirämisch. Das ergibt die Frage, ob wir hier möglicherweise ein Phänomen des „Re-Controllings“ ohne Therapie bei HIV-2 beobachten?
Zwei europäische HIV-2-Zentren, Paris und Lissabon, konnten dieses Phänomen nicht beobachten. In einer Rotterdamer Kohorte ist dagegen das Phänomen des „Re-Controllings“ bei unbehandelten PLWH2 berichtet worden (Hensley et al. 2025).
„Viraemic Controllers“
Wir haben unsere Gruppe der PLWH2, die keine Therapie brauchen, als „VC“ (Viraemic Controllers) klassifiziert. Die Klassifizierung in diese Gruppe wird erschwert durch die deutlich langsamere Standardisierung der Methoden zur HIV-2 Viruslastbestimmung und die erst in den letzten Jahren deutlich abnehmende Nachweisgrenze bei der HIV-2 PCR. Hinzu kommt, dass die größere Divergenz der genetisch unterschiedlichen Gruppen von HIV-2 die Entwicklung entsprechender Testverfahren erschwert, d.h. so niedrige Nachweisgrenzen wie bei HIV-1 im quantitativen Test konnten bisher nicht erreicht werden.
Krankheitsprogression
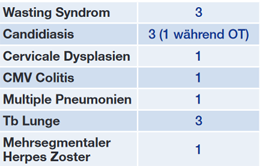
Tab. 1 Klinische Events (CDC B und C, zum Teil mehrere Events bei einem Individuum)
21 (84%) der Teilnehmenden in H2O bekommen eine ART. 13 Personen begannen mit der ART gleich bei Einschluss in die Studie, d.h. mit Beginn der Beobachtungszeit.
Sieben Teilnehmende präsentierten sich bei Erstdiagnose und Erstvorstellung mit klassischen HIV-assoziierten Symptomen (Tab. 1) und bekamen umgehend eine ART. Die CD4-Zellzahl lag im Mittel bei 98 Zellen/µl (8-220). Interessanterweise hatten drei Personen bei Erstdiagnose keine nachweisbare Virämie. Die anderen Teilnehmenden hatten eine Virämie von 100-22.000 Kopien HIV-2-RNA/ml.
Weitere sechs Teilnehmende ohne klinische Ereignisse, aber mit fortgeschrittenem CD4-Zell-Verlust (im Mittel 220 c/µl, 17-374), starteten die ART gleich bei Erstdiagnose und Erstvorstellung – drei Personen mit Virämie (1.000 bis 66.800 HIV-2 RNA cop./ml) und drei Personen ohne Virämie.
Acht Teilnehmende starteten später während der Beobachtungszeit. Eine Person davon wegen eines klinischen Events (oropharyngeale Candidiasis bei 412 CD4/µl und 120 HIV-2-RNA Kopien/ml) und fünf wegen wiederholter Virämie (HIV-2 RNA 50-22.000 Kopien/ml) und kontinuierlichem Abfall der CD4-Zellen auf im Mittel 345 Zellen/µl (Range 319-371).
Sonderfälle
Phylogenie von HIV-2
Die Gruppen bei HIV-2 wie A und B sind vergleichbar divergent wie Gruppe O und Gruppe M bei HIV-1 (wozu die üblichen zirkulierenden Subtypen wie B, C und A gehören) (Faria et al. 2013). Es existieren zwar zur Überprüfung der Sicherheit von Blutprodukten in den Blutbanken Tests mit vergleichbarer Empfindlichkeit wie für HIV-1, diese sind aber nicht für die Quantifizierung und damit das Therapiemonitoring geeignet.
Wir beobachten auch einige ungewöhnliche Verläufe wie Krankheitsprogression ohne Virämie. Eine Person mit HIV-2 Infektion zeigte über 15 Jahre bei klinischer Stabilität einen kontinuierlichen Abfall der CD4-Zellen von 786 auf 331 Zellen/µl, ohne jemals virämisch gewesen zu sein. Nach Start einer ART kam es innerhalb von 10 Jahren Therapie zu einem Anstieg der CD4-Zellen auf zuletzt 734 Zellen/µl. In einem anderen Fall entschieden sich Teilnehmende(r) und Behandler(in) bei wiederholt aufgetretenen Blips (HIV-2-RNA 100 Kopien/ml) und stabiler CD4-Zellzahl (>600/µl) für eine ART als TasP („Treatment as Prevention).
ART-Verlauf
Wenn man nur die Teilnehmenden bewertet, die in der Studie verblieben sind, liegt bei 16 von 18 Behandelten zum jetzigen Zeitpunkt ein gutes Behandlungsergebnis vor: 8/16 Teilnehmende sind noch erfolgreich unter ihrer First-Line-Therapie (mittlere OT 6,3 Jahre, alle starteten nach 2016, mit einen Zweitgenerations-INSTI). Der CD4-Anstieg war im Mittel 72 c/µl nach 12 Monaten und 156 c/µl nach 24 Monaten.2 Bei 7/16 Personen wurde im Laufe die ART auf einen Zweitgenerations-INSTI umgestellt, ohne dass ein Therapieversagen vorgelegen hat.3 Als Gründe wurden Nebenwirkungs- und Wechselwirkungsmanagement und Therapievereinfachung angegeben. Im Verlauf waren die CD4-Zellzahlen stabil und es gab keine klinischen Ereignisse (mittlere OT 13,6 Jahre). Bei 1/16 Personen sprach die 2004 begonnene ART mit einem bei HIV-2 nicht wirksamen NNRTI (NVP) nicht an. Nach Umstellung auf einen Zweitgenerations-INSTI kam es jedoch zu anhaltender virologischer Kontrolle und zu einem CD4-Zell Anstieg.
Auch bei dieser Gruppe der kontinuierlich behandelten PLWH2 sahen wir gelegentliche Blips, Low-Level-Virämien bis zu 12 Monate und sogar relevante Virämien (>1.000 Kopien/ml), gefolgt von Testergebnissen unter der Nachweisgrenze, ohne dass es eine Therapieänderung oder eine klinische oder immunologische Reaktion gegeben hätte.4
Therapieversagen
In 2/18 Fällen (OT 19 und 24 Jahre) kam es unter ART nicht zu einer dauerhaften Virussuppression und nicht zu einem dauerhaften CD4 Zellanstieg. Beide Teilnehmende hatten AIDS-Ereignisse bei Therapiestart und im Verlauf auch unter der ART.
Die Therapie wurde 1999 mit Indinavir begonnen und 2000 (Beginn der Beobachtungszeit) auf Amprenavir/r (beides nicht wirksam) umgestellt. Es folgte eine ineffektive Umstellung auf Triple-NUK. Im anderen Fall wurde mit Lopinavir/r begonnen. Grund für das Therapieversagen ist möglicherweise mangelnde Compliance. Mittlerweile haben beide Personen eine Multiklassenresistenz (Resistenzen gegen alle NRTI, PI, INSTI und in einem Fall sogar gegen Lenacapavir) erworben bei CXCR4-Tropismus.5 Beide Personen haben einen jetzt schon seit Jahren anhaltend bestehenden fortgeschrittenen Immundefekt mit weniger als 100 CD4-Zellen/µl. Eine effektive ART mit voll wirksamen und zugelassenen Substanzen kann für diese PatientInnen zurzeit nicht zur Verfügung gestellt werden.
Neue Leitlinie
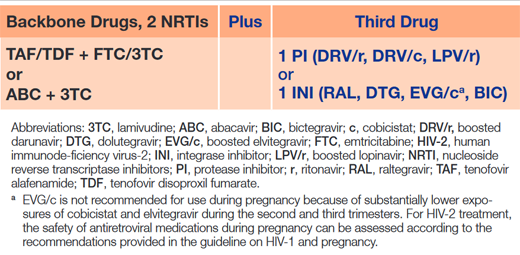
Tab. 2 Recommended Drugs for First- and Secondline Treatment of Persons Living With Human Immunodeficiency Virus-2 (Berzow et al. 2021)
Unsere
Daten aus der H2O-Kohorte konnten wir auch in die Aktualisierung des
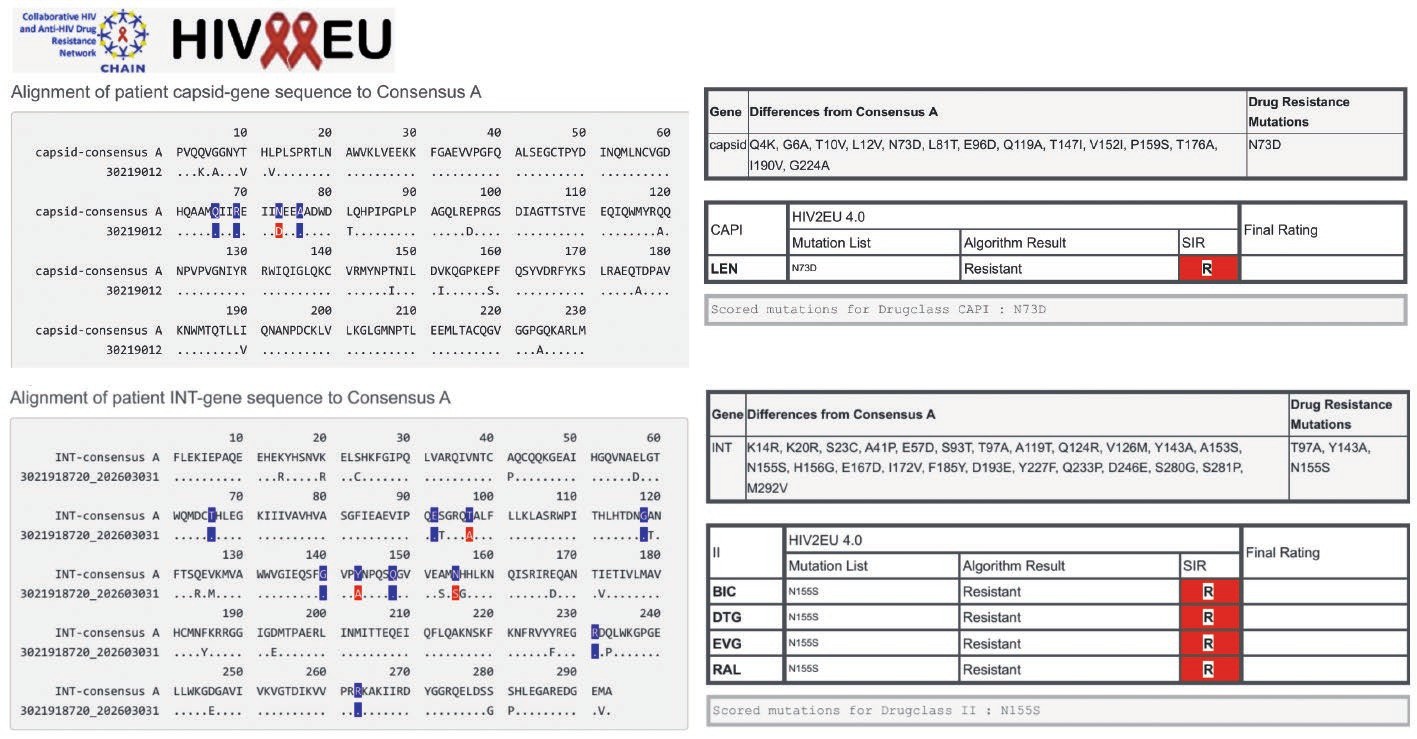
HIV-2EU-Regelwerkes einbringen. HIV-2EU (Update in: Charpentier et
al. 2025) ist eine Kooperation verschiedener Arbeitsgruppen aus
Frankreich (v.a. Diane Descamps, Charlotte Charpentier und Quentin Le
Hingrat), Portugal (v.a. Perpetua Gomes), den Niederlanden (v.a.
Jeroen van Kampen) und Deutschland. Ziel von HIV-2EU ist es, in-vitro
aber auch in-vivo Daten zur genotypischen Resistenzbestimmung für
HIV-2 zu sammeln und diese Erfahrung mittels eines Regelwerks für
die Interpretation von Sequenzen zu teilen. Ein dazugehöriges Tool
steht auf der Internet-Seite von HIV-GRADE (www.hiv-grade.de)
zur Verfügung. Das Regelwerk wird jährlich aktualisiert. So konnten
zuletzt auch Daten für Lenacapavir integriert
werden.
Neue Optionen
Lenacapavir zeigt eine gute Wirksamkeit bei HIV-2, wobei höhere Medikamentenspiegel als bei HIV-1 benötigt werden. Die Beurteilung weiterer HIV-1 wirksamer Medikamente als Therapieoption für HIV-2 wurde ebenfalls von der europäischen Arbeitsgruppe vorgestellt (Charpentier et al. 2025). Als weitere Therapieoption ist Ibalizumab zu erwägen, ein Medikament, für das die Zulassung in Europa aus wirtschaftlichen Gründen zurückgenommen wurde und das damit noch schwieriger verfügbar ist als Lenacapavir, welches derzeit in Europa ebenfalls nicht zur Verfügung steht. Fostemsavir zeigt keine Wirksamkeit bei HIV-2, was aufgrund der strukturellen Unterschiede im Hüllprotein zwischen HIV-1 und HIV-2 nicht verwunderlich ist.
Viel
Hoffnung liegt derzeit vor allem auf Islatravir. Islatravir ist als
Nukleosid-Analogon wirksam an der reversen Transkriptase. Es gibt
in-vitro sogar Hinweise auf eine im Vergleich zu HIV-1 höhere
Empfindlichkeit. Dies wäre für die HIV-2 Therapie ein immenser
Zugewinn, da Medikamente für HIV-1 sonst entweder keine Wirksamkeit
haben (NNRTI, einige Protease-Inhibitoren) oder eine geringe
Resistenzbarriere zeigen (Integrase-Inhibitoren,
Protease-Inhibitoren, NRTI) (Charpentier et al. 2025).
Anmerkungen
- Bei Teilnahme-Abbruch (LTFU) einmal Therapieansprechen, einmal Therapieversagen (immunologisch und virologisch), einmal Therapieansprechen unklar, nach Auftreten von klinischem Event (Candidiasis) und ART Einleitung Abbruch.
- Bei zwei Teilnehmenden mit niedrigen CD4 war der CD4 Anstieg nach 60 Monaten von 17 auf 190 c/l, bzw. 236 auf 444 c/µl.
- Der Switch erfolgte fünfmal von PI und je zweimal von einem Erstgenerations-INSTI. Bei einem Individuum in der PI Gruppe gab es anfangs einen sehr schnellen Switch: NNRTI (RPV) auf PI (LPV), nach 4 Wochen, dann 2014 dann 2024 auf INSTI, (#51/60, Ko-I.).
- Ein(e) Teilnehmende(r) hat eine permanente LLV:
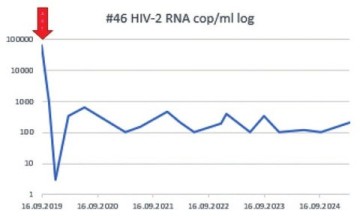
- Letzte Resistenzanalysen:
H2O11: NRTI K65R, V111I , M184V, PI I50V, I54M, I64V, INSTI T97A, Y143A, N155S, CI D67N. H2O12: NRTI: K65R, N69S, V111IV, Q151M, M184IMV, 223KR, PI : I54IM, I82FI, L90M, INSTI: E92A, N155H.
Unklar ist die Wirksamkeit von Maraviroc bei HIV-2. Der Wirkmechanismus ist nicht beeinträchtigt, HIV-2 scheint aber häufiger den CXCR4-Rezeptor als Corezeptor zu verwenden (Visseaux et al. 2015), was gegen den Einsatz eines CCR5-Blockers spricht. Ob dies grundsätzlich typisch für HIV-2 ist oder ob dies daraus resultiert, dass aufgrund des natürlichen Verlaufes der HIV-2 Infektion erst zu späten Zeitpunkten der Corezeptor-Tropismus getestet wird, ist unklar. Für HIV-1 Infektion ist bekannt, dass bei längerem Verlauf und fortgeschrittenem Immundefekt bzw. niedrigem CD4-Nadir der Anteil CXCR4-troper Viren zunimmt. Der klinische Verlauf der HIV-2 Infektion stellt daher auch in dieser Hinsicht eine besondere Herausforderung dar. In der Gruppe HIV-2EU wird u.a. auch aus diesem Grund intensiv über neue Methoden diskutiert, z.B. ob und wie die Umsetzung des derzeit für HIV-1 intensiv validierten intakten proviralen DNA Assays (IPDA) auf HIV-2 erfolgen kann und ob diese Technologie zum Nachweis infektionskompetenter integrierter viraler Genome eine prädiktive Kraft für das Erkennen der verschiedenen Verlaufsformen einer HIV-2 Infektion haben kann (Lu et al. 2022).
Fazit
Bei HIV-2 gibt es – wie auch unsere Studie H2O belegt – Krankheitsprogression ohne Virämie (Hensley et al. 2025). Aber gibt es auch Virämie ohne Krankheitsprogression? Die Daten und der Verlauf bei diesen „Viraemic Controllers“ und möglicherweise „Re-Controllers“ sind nicht leicht zu interpretieren. Sind es Laborartefakte oder handelt es sich hier um ein vielleicht HIV-2 spezifisches „Re-Controlling“? Ist es klinisch relevant? Können wir mit neuen Methoden zur Quantifizierung replikationsfähiger Virusgenome in der proviralen DNA die Bedeutung von geringen Virämien bei HIV-2 besser verstehen?
Bei der überwiegenden Mehrheit der PLWH2 in H2O läuft die Therapie gut und stabil, vor allem seit der Verfügbarkeit von Zweitgenerations-INSTI und einfach einzunehmenden Single-Tablet-Regimen.
Therapieversagen bei HIV-2 mit schnell erworbener MCR (Multi-Class-Resistance) stellt allerdings aufgrund der im Vergleich zu HIV-1 deutlich eingeschränkteren Therapieoptionen ein großes Problem dar.
Das
bisher Zusammengetragene führt zu mehr Fragen als Antworten.
Gleichzeitig gibt es uns aber auch viel Motivation, die Studie
weiterzuführen, weiter zu diskutieren, und durch Beteiligung von
zusätzlichen Zentren zu erweitern. Die H2O Studie ist ein
Investigator-Initiated Trial. Unser herzlicher Dank gebührt allen
Teilnehmenden und allen, die durch ihre
unentgeltliche
Mitarbeit die Studie möglich machen.
Berzow D et al. Human Immunodeficiency Virus-2 (HIV-2): ASummary of the Present Standard of Care and Treatment Options for Individuals Living with HIV-2 in Western Europe. Clin Infect Dis. 2021 Feb 1;72(3):503-509. doi: 10.1093/cid/ciaa275. PMID: 32227124
Charpentier C et al. 2025. HIV-2 EU-Supporting Standardized HIV-2 Drug Resistance Interpretation: An Update. Clin Infect Dis Off Publ Infect Dis Soc Am. 81(3):539-542. https://doi.org/10.1093/cid/ciaf110
Faria NR et al. Phylogeographic Insights into the Origins and Epidemic History of the Human Immunodeficiency Virus Type 2. In: Hope TJ, Stevenson M, Richman D, editors. Encyclopedia of AIDS. Springer New York; p 1-9 [accessed 2024 Apr24]. https://link.springer.com/10.1007/978-1-4614-9610-6_44-1. https://doi.org/10.1007/978-1-4614-9610-6_44-1
Hensley KS et al. 2025. Insights to a Cure: Unique Controller Phenotypes in the Rotterdam HIV-2 Cohort. Open Forum Infect Dis. 12(7):ofaf336. https://doi.org/ 10.1093/ofid/ofaf336
Lu MD et al. 2022. Novel assays to investigate the mechanisms of latent infection with HIV-2 Kashanchi F, editor. PLOS ONE. 17(4):e0267402. https://doi.org/10.1371/journal.pone.0267402
Visseaux B et al. 2015. Tropism distribution among anti-retroviral-naive HIV-2-infected patients. AIDS. 29(16): 2209.https://doi.org/10.1097 QAD.0000000000000825







 Diese Seite weiter empfehlen
Diese Seite weiter empfehlen