33rd Conference On Retroviruses And Opportunistic Infections (croi), Denver, Usa
 Nach dem
„Annus horribilis“ – es geht weiter!
Nach dem
„Annus horribilis“ – es geht weiter!
Die letzte CROI stand noch unter dem Schock der radikalen Schnitte der Trump-Regierung bei Hilfsprogrammen und Wissenschaft. Auch bei der Eröffnung dieser CROI kam das „Annus horribilis“ (Zitat des Aktivisten Peter Staley) zur Sprache, aber die Stimmung war anders. Während vor einem Jahr noch Schockstarre vorherrschte, sind jetzt Widerstand und Aufbruch zu spüren. Ein Zeichen dafür war unter anderem die Verleihung des neu geschaffenen „Lifetime Achievement Award“ an den früheren Direktor des National Institute of Allergy and Infectious Diseases (NIAID) Carl Dieffenbach – ein klares Zeichen gegen den aktuellen wissenschaftsfeindlichen Trend in den USA (und überall in der Welt).
Ante portas
Bei den klinischen Studien zu neuen Regimen gab es einige mehr oder weniger neue Daten, denn vielfach werden die wichtigsten Ergebnisse von den Herstellern schon vor dem Kongress publiziert. Neue Regime, zu denen Phase-3-Studien präsentiert wurden, und die in absehbarer Zeit zur Verfügung stehen werden, sind die Fixkombinationen Islatravir/Doravirin (ISL/DOR), Bictegravir/Lenacapavir (BIC/LEN) und Islatravir/Lenacapavir (ISL/LEN).
ISL/DOR
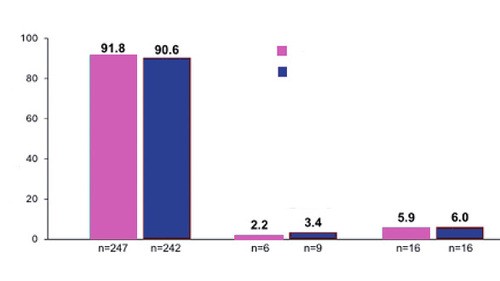
Abb. 1 Doravirin/Islatravir als Firstline. Virologisches
Ergebnis zu Woche 48
Islatravir/Doravirin (100/0,25 mg) QD als Firstline-Regie war bei therapie-naiven PLWH virologisch vergleichbar mit BIC/F/TAF. Nach 48 Wochen lag die Viruslast bei gleich vielen Personen unter der Nachweisgrenze – auch bei hoher Viruslast, niedriger CD4-Zellzahl und minoren NRTI- bzw. NNRTI-RAMs bei Therapiebeginn (Abb. 1). Ein virologisches Versagen mit Resistenzentwicklung wurde bei <1% (2/269) Personen beobachtet. Die Verträglichkeit war gleichermaßen gut. Die häufigsten Nebenwirkungen waren Gewichtszunahme (+3,5 kg vs +3,9 kg), Kopfschmerz (2,2% vs 3,4%), eGFR-Abfall (0,7% vs 3,0%) und Blähungen (0,4% vs 2,2%). Drei Patienten unter dem dualen Regime infizierten sich mit Hepatitis B, was die Notwendigkeit eines entsprechenden Impfschutzes unterstreicht (Rockstroh K et al., #177).
Zum Switch auf ISL/DOR wurde ein Update von zwei Studien vorgestellt. In der einen Studie wurden supprimierte PLWH von BIC/F/TAF, in der anderen von einem nicht definierten Regime entweder umgestellt oder weiterbehandelt. Die virale Suppression blieb in beiden Studien mit >90% gleichermaßen hoch und auch die Verträglichkeit war vergleichbar (Orkin C et al., #515; Colson A et al., #514).
BIC/LEN
Die Kombination Bictegravir/Lenacapavir QD wurde im Switch-Setting geprüft an supprimierten, aber stark vorbehandelten PLWH auf einem komplexen Regime. Präsentiert wurden die 48 Wochen Daten der beiden Phase-3-Studien ARTISTRY-1 (n=729) und ARTISTRY-2 (n=574) sowie die 96 Wochen Daten der Phase-2-Studie präsentiert. Die Teilnehmenden waren in der Regel sehr lange behandelt (Jahrzehnte), nahmen viele Tabletten (bis zu 11 Tabletten/d) und sehr viele hatten Resistenzen (bis zu 80%). In ARTISTRY-1 wurde auf BIC/LEN QD umgestellt oder weiterbehandelt. In ARTISTRY-2 wurde auf BIC/LEN oder B/C/TAF jeweils QD umgestellt. Die virologische Wirksamkeit war vergleichbar, ebenso die Nebenwirkungsrate. Bei vier Personen wurde eine Viruslast <1.000 K/ml beobachtet. Bei 1/4 unter BIC/LEN wurde zu Woche 36 eine INSTI-Mutation (R263K) ohne phänotypische Resistenz detektiert. An der Verlängerung des BIC/LEN-Armes von ARTISTRY-2 nahmen 52 Personen teil. In den 96 Wochen kam es zu keinem viralen Durchbruch, es wurde keine Resistenz beobachtet (Orkin C et al., #181; Meissner EG et al., #513; Hedgcock M et al., #518).
Die Prävalenz von Resistenzmutationen gegen Lenacapavir ist, so die Analyse der Los Alamos HIV Database aktuell sehr niedrig (Q67H oder M66I <1%). T107N allein und insbesondere in Kombination mit anderen RAMs vermindert die Wirksamkeit von Lenacapavir. Die Kapsid-Polymorphismen T107A und T107S haben dagegen keinen Einfluss (Begovic E et al., #579; Nicolas M et al., #581).
ISL+LEN
Zur Kombination ISL+LEN wurden die 96-Wochen-Daten einer Switch-Studie vorgestellt. Alle Teilnehmenden (n=97) waren komplett supprimiert und wurden auf ISL 2 mg+LEN 300 mg 1QW oder BIC/F/TAF QD umgestellt. Wirksamkeit und Verträglichkeit beider Regime waren gleichermaßen gut, kein negativer Einfluss auf Lymphozyten oder CD4-Zellen. Die Adhärenz bei dem einmal wöchentlichen Tabletten Regime war mit fast 99% sehr gut. Die Resistenzanalyse ergab keine Therapie-assoziierten Mutationen. Auch zwei Patienten mit früherer M84V/I blieben unter der Nachweisgrenze. Die Phase-3-Studien mit der Fixkombination ISL/LEN ISLEND-1 und -2 laufen bereits (Colson A et al., #516; Bekermann E et al., #586).
Zukunft
Noch keine Heilung, aber doch eine längere Medikamenten-frei Zeit könnte die Kombination von breit neutralisierenden
Antikörpern mit langwirksamen antiretroviralen Substanzen bringen. In der EMBRACE-Studie wurden supprimierte PLWH
(n=125), deren Virus sensibel für den bnAB Lotivibart (LBV, N6LS) war, mit LBV IV oder SC und Cabotegravir-LA jeweils
Q4M IM oder mit dem alten Regime behandelt. Zu Monat 12 waren von den Teilnehmenden 94% unter LBV IV, 82% unter LBV SC
und 88% unter dem alten Regime unter der Nachweisgrenze. Die Verträglichkeit war gut, mehr Nebenwirkungen gab es bei der
subkutanen Injektion von LBV (53% vs 24%). In der bereits laufenden Studie EMBRACE 2 wird allerdings eine andere
Dosierung geprüft: LBV IV Q6M + LA CAB IM Q2M (Rolle CP et al., #178) (Abb. 2).
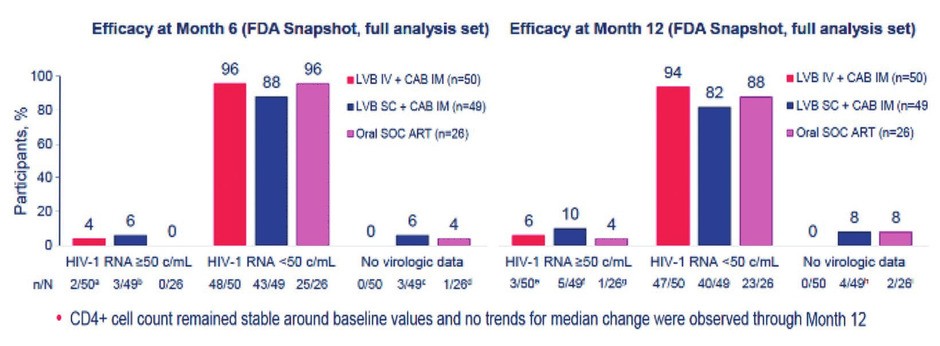
Abb. 2 LVB+CAB IM Maintained
Virologic Suppression in a High Proportion of Adults with Baseline LVB Sensitivity
Die Kombination Lenacapavir plus die bnABs Teropavimab (TAB) und Zinlirvimab (ZAB) wird zur zweimal jährlichen Gabe entwickelt. Vorgestellt wurde die Resistenzanalyse zu Woche 52. 2/53 Personen wurden resistent gegen den Antikörper ZAB, eine davon entwickelte auch eine Resistenz gegen Lenacapavir (VanderVeen LA et al., #567). Die Patienten waren mit dem Regime sehr zufrieden (Price K et al., #517).
Nicht weiter geht es dagegen mit dem neuartigen Ansatz die zwei Immunmodulatoren Budigalimab (PD1-Inhibitor) plus Trosunilimab (anti-alpha-4 beta-7 Integrin Rezeptor) zu kombinieren. In der Phase-2-Studie (n=142) traten trotz niedriger Dosierung gravierende Nebenwirkungen auf (Pires Dos Santos, A et al., #140).
Ferne Zukunft
Der Trend geht zu „Ultralong Acting“. Hier sind einige Substanzen in der Pipeline zur Therapie wie auch zur PräExpositionsProphylaxe (PrEP). CAB-ULA 1.600 mg ist ein Kapsid-Inhibitor der einmal alle 4 Monate appliziert wird (Castronova E et al., #495). GS-3242 ist ein langwirksamer INSTI mit einer Wirkdauer über mindestens 4 Monate (Gupta S et al., #174). VH-184 ist ein INSTI der 3. Generation mit dem Potential für eine zweimal jährliche Applikation subkutan bzw. intramuskulär (Underwood M et al., #554). VH-499 ist ein Kapsid-Inhibitor ebenfalls mit dem Potential für zweimal jährliche Injektion (Thakkar N et al., #492). Doravirin wird zu einem Implant entwickelt (Benhabbour SR et al., #494).
Gegenwart
Wie immer gab es viele Studien mit „real world“-Daten zu den zugelassenen Regimen in verschiedenen Populationen, Situationen und Regionen. In der Studie VOLITION wählten 129/151 therapienaive PLWH, die nach Einleitung der ART mit Dolutegravir/3TC innerhalb von 4-16 Wochen komplett supprimiert waren, den Switch auf CAB/RPV-LA. Gründe für die Wahl waren Angst Tabletten zu vergessen, Reisen und Convienence (Rolle C-P et al., #525).
Mehrere Arbeiten verglichen CAB/RPV-LA mit oraler ART bei virämischen Patienten mit Adhärenzproblemen. Sowohl in den Kohorten wie auch in einer prospektiven taiwanesischen Studie (n=45) (Chen NY et al., #530) schnitt die Injektionstherapie besser ab.
PrEP
Die PrEP mit Lenacapavir subkutan Q6M ist ohne Zweifel ein großer Durchbruch. Bei der ersten Präsentation der Daten hatten 50% der Teilnehmenden Woche 48 erreicht. Jetzt haben alle zu Woche 65 das Ende der blinden Phase erreicht. In PURPOSE-1 (n=5.345 junge afrikanische Frauen) gab es bei der ersten Auswertung keine HIV-Infektion unter LEN. Zu Woche 65 wurden zwei HIV-Infektionen (0,07/100 PY) beschrieben. Eine Patientin wurde in Woche 65 positiv getestet, die PCR war retrospektiv bereits zu Woche 52 positiv, der LEN-Spiegel war ausreichend hoch. Die zweite Patientin war zur zweiten Injektion zu Woche 52 nicht erschienen. Der HIV-Test war zu Woche 65 positiv, also 16 Monate nach der letzten LEN-Injektionen.

Abb. 3 HIV Incidence and Resistance in LEN-Randomized Participants
During PURPOSE 1 and PURPOSE 2© FireflyGeminiPauli
In PURPOSE-2 (n=3.271 MSM und Transgender) wurden zu Woche 52 unter LEN drei HIV-Infektionen beobachtet. Zu Woche 65 kam unter LEN eine weitere HIV-Infektion hinzu. Der junge transgender MSM hatte alle Injektionen erhalten und einen ausreichenden Spiegel. Von den insgesamt fünf Personen, die sich unter LEN-PrEP mit HIV-Infizierten hatten, hatten 3/5 die Kapsid-RAM N74D und 1/5 zusätzliche eine K70R entwickelt (Abb. 3) (Ndlovu N et al., #128; Cantos VD et al., #129: COX S et al., #130).

Kongresszentrum Denver. CROI 2026: Sonnenaufgang oder Sonnenuntergang?
In den USA ist CAB-LA Q2M zur PrEP zugelassen. In der OPERA-Kohorte wurden die Daten von PrEP-User mit ≥1 CAB-LA von 12/2021 bis 12/ 2024 (n=1.748) ausgewertet. In diesen ersten drei Jahren kamen 59% rechtzeitig zur Injektion, 85% im Schnitt vier Tage zu spät. Bei 15% musste die PrEP neu gestartet werden, 32% brachen ab. Im ersten Jahr nach PrEP-Start wurde bei einer Person unter CAB-LA eine HIV-Infektion diagnostiziert. Der User hatte keinen HIV-Test vor Beginn (Brunet L et al., #979 und #980).
Eine Alternative zur Spritze und täglichen Tablette könnte das NNRTI MK-8527 sein, das als eine Tablette pro Monat zur PrEP entwickelt wird. Die Dosierung von 11 mg 1QM hat sich als ausreichend erwiesen und hat ein Forgiveness-Fenster von einer Woche. Die Phase-3-Studien EXPrESSIVE-10 und -11 laufen bereits (Kapoor Y et al., #126).







 Diese Seite weiter empfehlen
Diese Seite weiter empfehlen